La EM es una enfermedad crónica, inflamatoria, desmielinizante y neurodegenerativa del SNC, que conduce a una pérdida creciente de la función física y cognitiva.1
La enfermedad se caracteriza por discapacidad neurológica y puede tomar una de tres presentaciones clínicas principales: EMRR, EMSP y EM primaria progresiva (EMPP).1
Para alrededor del 85% de los pacientes, las recaídas son la expresión clínica exclusiva de la EM durante la presentación inicial y esto define la fase recurrente-remitente (EMRR). En la EMRR, las recaídas ocurren seguidas de una recuperación completa o parcial que conduce a la acumulación de discapacidad con el tiempo. Entre las recaídas, los pacientes con EMRR son clínicamente estables y tienen una exacerbación mínima de la discapacidad, es decir, entre recaídas existe una progresión de la enfermedad que no es aparente.2 Mientras que la mayoría de los pacientes con EMRR son diagnosticados entre las edades de 20 y 40 años, un pequeño número de pacientes son menores de 18 años.3 Con el tiempo, los pacientes con EMRR experimentan la transición a un curso secundario de enfermedad progresiva (EMSP). Los pacientes con EMSP presentan un empeoramiento gradual e irreversible de la discapacidad (como lo indica un puntaje EDSS creciente) el cual puede presentarse independientemente de las recaídas, lo que lleva a una mayor dependencia y asistencia para caminar.

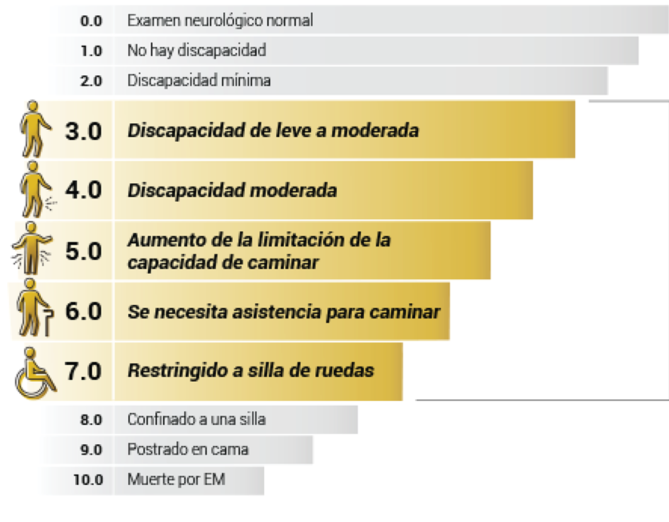
La escala ampliada del estado de discapacidad de Kurtzke (EDSS), una escala que abarca ocho sistemas funcionales (visual, tronco encefálico, piramidal, cerebeloso, sensorial, intestinal y vesical, cerebral y 'otro'), además de considerar directamente la movilidad. 4EDSS se considera la medida estándar de discapacidad en la práctica clínica, ensayos clínicos, evaluación de tecnologías sanitarias y modelos económicos.5-8
En términos generales, un valor en la escala EDSS ≤3 indica que paciente presenta una ambulación independiente con una discapacidad mínima, un valor de 4 a 6.5 indica una restricción en la movilidad requiriendo posiblemente algún elemento de apoyo para la movilidad, mientras que un puntaje ≥7 representa un alto nivel de apoyo requerido para la realización de actividades cotidianas.7
En la actualidad, no se han identificado criterios clínicos, de imagen, inmunológicos o patológicos claros para determinar el punto de transición a EMSP. De acuerdo con los criterios revisados de 2013 para definir el curso clínico de la EM, los fenotipos de EM recurrentes y progresivos se pueden clasificar de acuerdo con la presencia de recaídas y/o actividad de resonancia magnética.12
- Forbes, R. B., Lees, A., Waugh, N., & Swingler, R. J. (1999). Population based cost utility study of interferon beta-1b in secondary progressive multiple sclerosis. British Medical Journal, 319(7224), 1529-1533. Retrieved from http://www.embase.com/search/results?subaction=viewrecord&from=export&id...
- Graham, B., & McGregor, K. (1997). What does a GP consultation cost? The British journal of general practice : the journal of the Royal College of General Practitioners, 47(416), 170-172. Retrieved from https://www.ncbi.nlm.nih.gov/pubmed/9167322
- https://www.ncbi.nlm.nih.gov/pmc/PMC1312925/
- Grima, D. T., Torrance, G. W., Francis, G., Rice, G., Rosner, A. J., & Lafortune, L. (2000). Cost and health related quality of life consequences of multiple sclerosis. Mult Scler, 6(2), 91-98. doi:10.1177/135245850000600207
- Hartung, H. P., Gonsette, R., Konig, N., Kwiecinski, H., Guseo, A., Morrissey, S. P., Zwingers, T. (2002). Mitoxantrone in progressive multiple sclerosis: a placebo-controlled, double-blind, randomised, multicentre trial. Lancet, 360(9350), 2018-2025. doi:10.1016/s0140-6736(02)12023-x
- Henriksson, F., Fredrikson, S., Masterman, T., & Jönsson, B. (2001). Costs, quality of life and disease severity in multiple sclerosis: A cross-sectional study in Sweden. European Journal of Neurology, 8(1), 27-35. doi:10.1046/j.1468-1331.2001.00169.x
- Holmes J, Madgwick T, & D, B. (1995). The cost of multiple sclerosis. Br J Med Econ, 8, 181–193.
- Kobelt, G., Jönsson, L., Henriksson, F., Fredrikson, S., & Jönsson, B. (2000). Cost-utility analysis of interferon beta-1b in secondary progressive multiple sclerosis. International Journal of Technology Assessment in Health Care, 16(3), 768-780. Retrieved from http://www.embase.com/search/results?subaction=viewrecord&from=export&id...
- Kobelt, G., Jönsson, L., Miltenburger, C., & Jönsson, B. (2002). Cost-utility analysis of interferon beta-1b in secondary progressive multiple sclerosis using natural history disease data. International Journal of Technology Assessment in Health Care, 18(1), 127-138. Retrieved from http://www.embase.com/search/results?subaction=viewrecord&from=export&id...
- Orme, M., Kerrigan, J., Tyas, D., Russell, N., & Nixon, R. (2007). The effect of disease, functional status, and relapses on the utility of people with multiple sclerosis in the UK. Value in Health, 10(1), 54-60. doi:10.1111/j.1524-4733.2006.00144.x
- Parkin D, M. P., McNamee P, Thomas S, Jacoby A, Bates D. (1998). A cost-utility analysis of interferon beta for multiple sclerosis: NIHR Health
CL2004819500 /AG2009216046

