Nuevo resumen EHA: Tratamiento con asciminib (SCEMBLIX®) llevó a respuestas rápidas y profundas en pacientes con LMC-FC con intolerancia o falta de eficacia con ≥2 ITCs
Las respuestas fueron rápidas con SCEMBLIX® y se continuaron profundizando en el tiempo, independiente de los niveles BCR::ABL1IS basales1
En pacientes con BCR::ABL1IS ≤10% en la línea basal:1
> 63.3% logró BCR::ABL1IS ≤1% a las 12 semanas y aumentó a 78.3% a las 96 semanas.
> 30.0% logró MMR a las 12 semanas y aumentó a 60.0% a las 96 semanas.
Figura. Incidencia acumulada de MMR ajustada para riesgos competitivosa y por niveles BCR::ABL1IS basales1
BCR::ABL1IS basal <10%
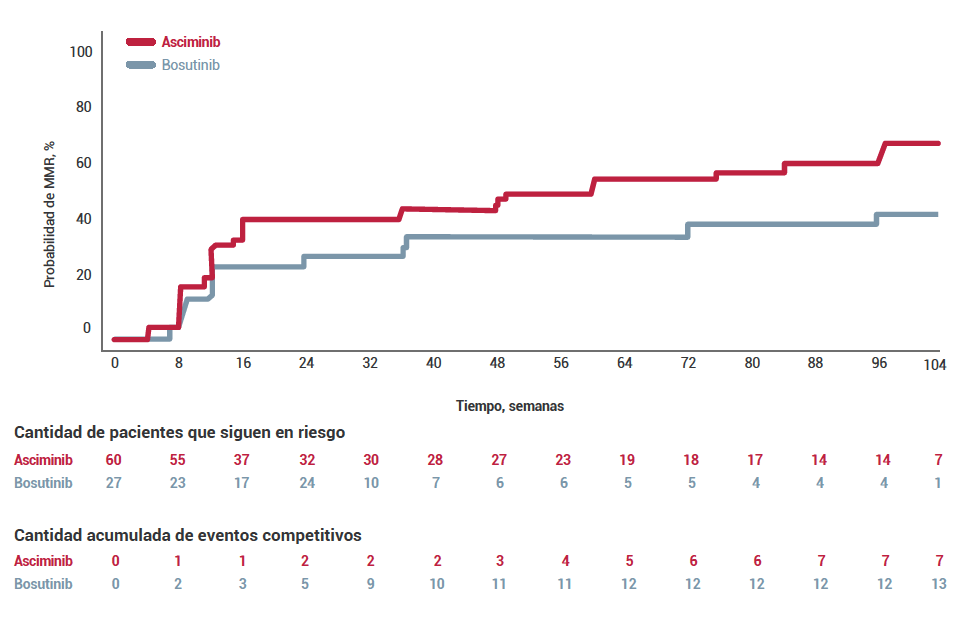
En pacientes con BCR::ABL1IS >10% en la línea basal:1
> 28.9% logró BCR::ABL1IS ≤1% a las 12 semanas con tasas similares a las 96 semanas.
> 10.3% logró MMR a las 12 semanas y aumentó a 23.7% a las 96 semanas.
BCR::ABL1IS basal ≥10%
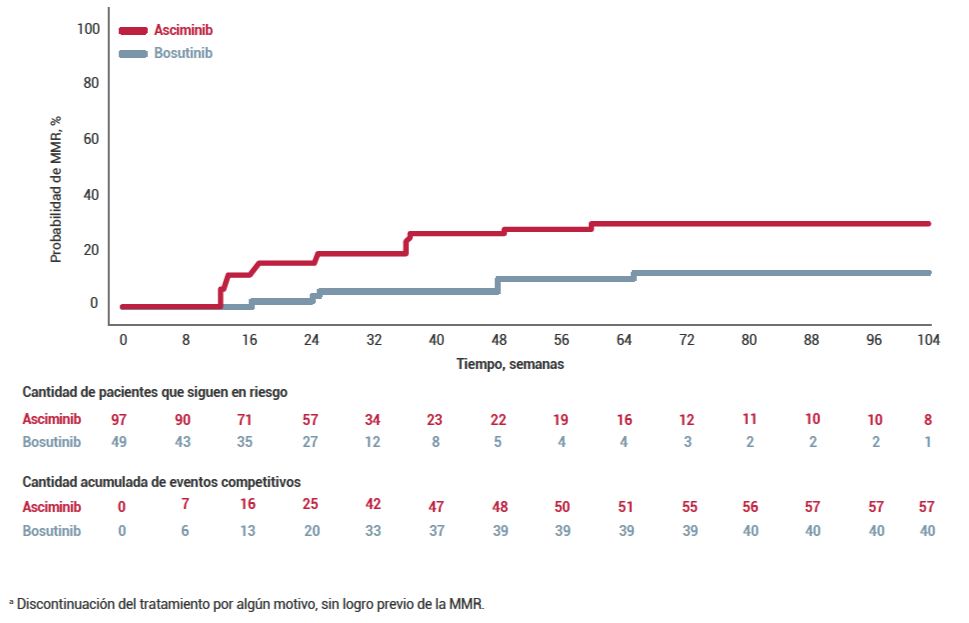
Los pacientes sin MMR a la semana 24 que permanecieron con SCEMBLIX® aún podrían alcanzar la MMR en puntos de medición posteriores1
• La probabilidad (IC 95%) fue de 17.9% (9.1%-29.0%) a 1 año y 37.9% (25.1%-50.6%) a los 2 años
Las tasas MMR totales en la semana 96 fueron mayores con SCEMBLIX® que con bosutinib, independiente del último ITC y el motivo para su discontinuación.1

Los resultados mostrados provienen de un análisis exploratorio de ASCEMBL, un estudio de 233 adultos con LMC-FC Ph+, tratados previamente con ≥2 ITCs: 157 pacientes recibieron SCEMBLIX® 40 mg bid y 76 pacientes recibieron bosutinib 500 mg qd hasta que ocurriera toxicidad inaceptable o falla terapéutica. 1,2
Acceder al Resumen científico
bid, 2 veces al día; LMC, leucemia mieloide crónica; IS, escala internacional; MMR, respuesta molecular mayor (BCR::ABL1IS ≤0.1%); LMC-FC Ph+, leucemia mieloide crónica en fase crónica positiva al cromosoma Filadelfia; qd, 1 vez al día.
Referencias: 1. Hughes TP, Réa D, Boquimpani C, et al. Rapid an d deep responses with asciminib in patients with chronic myeloid leukemia in chronic phase (CML-CP) after ≥2 prior tyrosine kinase inhibitors (TKIs) in the phase 3 ASCEMBL Study [Abstract P665]. Available on EHA Library. Accessed May 30, 2023. 2. Departamento de Registro Farmacéutico, Información básica para la prescripción de Scemblix® (asciminib). Última versión aprobada por el Instituto de Salud Pública de Chile 2022.
SERVICIOS DE INFORMACIÓN MÉDICA PARA PROFESIONALES DE LA SALUD
Material para uso exclusivo del profesional de la salud. Prohibida su exhibición y/o entrega a pacientes, consumidores y/o al público en general.

